第14回:薬剤耐性のはなし
最近、 "多剤耐性アシネトバクター"、"多剤耐性緑膿菌"など、「薬剤耐性」という言葉を耳、目にすることがしばしばあります。前回のコラム欄で「スーパー耐性菌。アシネトバクター バウマニ」を取り上げ多くの薬剤に耐性で感染した場合は治療が困難になるということを説明しましたが、すぐ後で某大学病院の院内感染が報道され、患者数人がその菌が原因で亡くなった可能性があることや他の病院でも詳細に調べたところ同様の患者が存在し感染制御に関する対応の遅れが指摘され、さらに別の新型の多剤耐性肺炎桿菌もみつかりさまざまな多剤耐性菌に対する対応方法の早急な確立などが指摘されています。
今回もこの「多剤耐性菌」を取り上げ一般的な話として、それらはどのようにして出現するのか、それらの耐性細菌が感染症にどのような影響を与えるのかなどについてコメントしたいと思います。またインド、パキスタン由来と言われている新たなタイプのNDM-1遺伝子保有耐性菌はさらに困った問題の原因になることについても説明します。
「薬剤耐性」とは
薬剤とは治療に使う化学療法剤(サルファ剤)と抗生物質のことを言います。このうち抗生物質とは放線菌や真菌(カビ)などの微生物が作った抗菌作用のあるものを精製したものですが、現在は化学的に合成したものが大部分です。また耐性とは、それらの薬剤が効かなくなったということで、その原因には(1)細菌の構造からもともと薬剤が効かない場合(自然耐性)と、(2)細菌の性質が変わって効かなくなった場合(獲得耐性)の2つがあります。したがってある感染症の原因となっている微生物がこの性質を持っていたとすると、その薬剤は治療に使っても効果が低いか、無効であることを意味します。ですから感染症の治療には原因病原体を検出したうえで、その病原体に有効と考えられる薬剤に対する効きかたを試験し(感受性試験といいます)、その結果をみて投薬する薬剤を決めれば良いのですが、検査で原因の病原体を検出するのに数日かかり、それを使って有効な薬剤を試験するとさらに日時がかかります。そこで患者の痛みや下痢、発熱などの苦痛を早く和らげるため、喫食調査や症状などと、これまでの経験から病原体を推定し、その病原体や類似細菌に効果がある薬剤(広域抗生物質=広い抗菌スペクトラム保有薬剤)を投与することが普通に行われています。効果があれば原因が何であれ、症状が軽快し、早期に治ることになりますが、効果が無いか、弱いかの時には耐性菌を出現させる原因となりますので乱用は避けなければなりません。この薬剤使用による原因はヒトだけの問題ではなく、動物治療薬としての使用や畜産、養鶏など動物飼料や養魚産業への疾病予防や肥育促進目的の添加使用も原因となっています。
薬剤耐性の問題はエイズウイルス、インフルエンザウイルスなど各種ウイルスでもみられますが、ここでは細菌について述べます。
「薬剤耐性の機序」
新しい抗生物質が使われ出すと一年以内には耐性菌が検出されるようになることが多いのですが、どのようにして薬剤に耐性となっているのでしょうか。次の方法が分かっています。
細菌が薬剤の分解や修飾する方法を獲得する
薬剤を分解したり構造を化学的に変化させる酵素を作り、それによって薬剤の効果を無くす。MRSAなどはペニシリナーゼやβラクタマーゼという薬剤分解酵素を産生してペニシリン系やセフェム系の薬剤を分解する。
細菌が薬剤の結合する作用点を変化して増殖可能とする
細菌自身が分子構造を変異して、それまで有効であった薬剤の作用点を無くす。ウイルスの薬剤耐性はほとんどこの機構によっている。
細菌が薬剤を菌体外へ排出する方法を獲得する
細菌がもっているエネルギーを用いて薬剤を細胞外に排出することで、細胞内の薬物濃度を下げ、効果を無くす。
その他の方法による耐性獲得法
化学療法剤のサルファ剤は、細菌の発育に必要な葉酸を合成するための前駆体を作る酵素に化学構造が似ており本物より先に結合し葉酸合成を阻害し、抗菌性を示すが、細菌が本来の前駆体酵素の構造を変えてサルファ剤が結合しなくして効果をなくす(耐性になる)。
結核菌などのミコバクテリウム属菌は、菌体の表面にミコール酸と呼ばれる特有の脂質が厚く覆っており薬剤が細胞壁を通過し菌体内に侵入するのを防ぐ。(消毒薬についても抵抗する効果がある)
「多剤耐性の獲得」
薬剤に耐性となる上記のような性質を獲得するにはどのような方法があるのでしょうか。主に次の2つがあります。
細菌自身の遺伝子が突然変異によって変化する
細菌が分裂増殖していく間に自身の染色体が突然に変異して、薬剤に耐性となる細胞が発生することがある。これは細菌を含め全生物が増殖するときには薬剤耐性だけではなく別の性質についても必ず起こっており、避けられないものです。
薬剤に対する変異はいきなり高濃度に耐性になるより段階的に耐性値(濃度)が上昇することのほうが起こりやすく、起こる頻度は薬剤の種類によって異なります。いきなり高濃度耐性になったのを確認できる(いわゆる薬剤耐性菌とされる)のは106~8個に1個程度の出現頻度と言われます。従って2剤に同時に耐性となる率は106 x 106=1012に1個、3剤には106 x 106 x 106=1018に1個で極めて低い頻度で現実には起こりえません。しかし低濃度耐性になったものがその後、薬剤の存在下で選択され増殖し、次第に高濃度になって行って高濃度耐性菌となることがあります。この機序による耐性の性質は下記の接合では伝達されず、耐性菌の出現は単剤(1つ)を使用した場合に起こりやすいので、耐性菌を出さないように(出現頻度を低下するために)有効な薬剤を2剤、3剤を併用して使用します。
細菌が薬剤耐性遺伝子を獲得する
"この機序による耐性化が多くの問題の原因となります"
細菌が生きていくためには必要ではない薬剤に関する遺伝子部分(領域)だけを持っている外来性遺伝子が新たに細胞内に侵入して一度に複数の薬剤に耐性の性質を獲得します。
この機序については下記「耐性遺伝子の受け渡し」で説明します。
「耐性遺伝子の受け渡し」
多剤耐性の遺伝子は一つの遺伝子上に耐性となる薬剤の遺伝子全てが存在しており、他の細菌にその遺伝子を受け渡し(伝達性のある)できる性質を持っているプラスミドと呼ばれるもので、とくに薬剤耐性プラスミド(R因子;Resistance factorまたはRプラスミド;R plasmid)といわれ、単剤から多剤の色々な耐性型があります。Rプラスミドは近縁の細菌間では高頻度で伝達されます(腸内細菌科の菌同士では100個に1個程度の割合で耐性菌が確認される)。従って感受性であった細菌がRプラスミドを獲得すれば一挙に7剤や8剤などに耐性となります。先に述べた突然変異による耐性化ではこのような高頻度で多剤耐性になることはなく、明らかに違っています。どの薬剤に耐性になるかはプラスミド上に存在する薬剤耐性遺伝子によって決まります。このような多剤耐性Rプラスミドが病原細菌をはじめ、多種類の細菌が保有していることが確認されており拡大に注意が必要です。
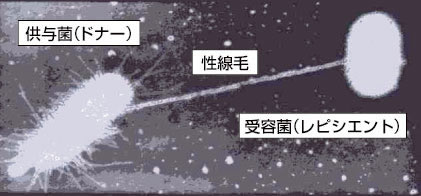
受け渡しの方法ですが、(1)薬剤耐性プラスミドを保有する細菌(供与菌:ドナー)から性線毛がのびて感受性菌(受容菌:レシピエント)に接合(conjugate)して行われる(図参考)と、(2)バクテリオファージ(細菌寄生性ウイルス)が薬剤耐性菌に感染し、細菌が持っている薬剤耐性遺伝子の一部を切り取って遺伝子を組み込んだファージが別の細菌に感染することによって、新たに薬剤耐性の遺伝子が持ち込まれて耐性を獲得する形質導入(transduction) という2つの方法が主なものです。
耐性遺伝子以外を含めて、どちらの方法も自然界でかなりの頻度で起こっていると考えられます。
「近年問題の多剤耐性細菌」
最近は大きく次の2グループの薬剤耐性菌が注目されています。
(1)- 5)結核菌以外はどれも感染に対する抵抗力が減少したヒトへの日和見感染原因細菌で治療薬が少ないことから問題となっています。
(1)臨床上問題の各種多剤耐性菌
メチシリン耐性黄色ブドウ球菌(MRSA);ペニシリン系のメチシリンに耐性の黄色ブドウ球菌を言いますが実際には多くの薬剤に耐性を示す多剤耐性菌である。mecA遺伝子を獲得し、セファロスポリン系などβ-ラクタム系薬剤に耐性を示す。この菌の代表的な治療薬はバンコマイシン、アルベカシン、テイコプラニンなどが第一選択薬剤となっています。
バンコマイシン耐性黄色ブドウ球菌(VRSA);バンコマイシン耐性遺伝子(vanA)を獲得して耐性化する((3)VREと同じプラスミド)
バンコマイシン耐性腸球菌(VRE);バンコマイシン耐性遺伝子(vanA)を獲得.輸入鶏肉や豚肉から検出されたという報告があります。
多剤耐性緑膿菌(MDRP);緑膿菌の治療薬であるイミペネム(カルバペネム系)、アミカシン(アミノ配糖体)、シプロフロキサシン(フルオロキノロン系)の3薬剤に耐性となったものをいう。
多剤耐性結核菌(MDR-TB)、超多剤耐性結核菌(XDR-TB)、多剤耐性結核菌(Multi Drug-resistant TB; MDR-TB);INH、RFPを含む2薬剤以上に耐性を示す。
超多剤耐性結核菌(Extensively Drug-resistant TB; XDR-TB);MDR-TBで、第二選択薬であるカナマイシン(KM)や、キノロン系薬剤にも耐性を示す。
多剤耐性アシネトバクター バウマニ(MRAB);コラム欄第13回を参照してください。
(2)新型の薬剤耐性菌―大腸菌と肺炎桿菌―
栃木県、獨協医科大学病院で前年入院した患者からNDM-1(New Delhi metallo lactamase-1,ニューデーリ・メタロ・ラクタマーゼ)という多剤耐性遺伝子を持つ大腸菌(Escherichia coli)が検出されたという記事が出ました。
福岡県、2008年4月に米国・ニューヨークの病院から転院してきた急性骨髄性白血病の患者(女性,35歳)の尿からカルバペネマーセ(KPC)という酵素を作る肺炎桿菌(Klebsiella pneumoniae)が検出されました。
両方の細菌はわが国では初めての経験で、最近、欧米諸国で患者発生が相次ぎ、死者も多数出ていることから世界的な問題としてWHOが監視の必要性を述べています。わが国でも厚労省が医療機関に通知し、汚染実態の調査をすることになっています(2010年9月以降)。
このNDM-1遺伝子、KPC遺伝子はプラスミド上にあり、これらの大腸菌や肺炎桿菌から両菌に近縁である他の腸内細菌科、とくに病原性の強い3類感染症に分類されているチフス菌、パラチフス菌、赤痢菌、腸管出血性大腸菌などへきわめて高頻度で多剤耐性遺伝子を伝達させ耐性化させるので、それに感染した患者の治療に使用可能な薬剤が無くなることを考えると深刻な問題です。
「とくにNDM-1薬剤耐性が深刻である点」
上記したMRSAやMDRPなどの薬剤耐性菌は感染症の治療によく使われているペニシリン系、セフェム系のβ-ラクタム剤をβ-ラクタマーゼという酵素(ペニシリナーゼ、セファロスポリナーゼという)によって分解し殺菌効果を無くさせることから、限られた治療薬しかないことが問題となっています。ところがNDM-1という耐性プラスミドはメタロβ-ラクタマーゼという酵素を作る遺伝子で、先の薬剤に加えてカルバペネム系などのβ-ラクタム系薬剤のほとんどを加水分解する酵素をつくります。カルバペネムはβ-ラクタム系薬剤に耐性の細菌による重症感染症の治療では「最後の手段」といわれている薬剤でこれに耐性になると治療薬がなくなるということから懸念されています。またNDM-1による耐性菌はグリコペプチド系(バンコマイシンなど)、アミノグリコシド系(ストレプトマイシン、カナマイシンなど)やニューキノロン系(レボフロキサシン、エノキサシンなど)薬剤にも同時に耐性となっており、β-ラクタマーゼの作用を無くす阻害剤もメタロβ-ラクタマーゼには効果がなく、まさに使える薬剤が無い"超スーパー耐性菌"です。
これまでの報告では、NDM-1耐性菌は抵抗力の減弱したヒトでの日和見感染菌(平素無害菌)にみられているだけで、健康なヒトの感染症を起こす病原細菌ではみつかっていませんので、早急にこの耐性遺伝子の拡散を防ぐ対策を確立し,汚染状況監視が必要です。
「薬剤使用上の注意」
カルバペネム系抗生物質は、非常に広い抗菌スペクトラムをもっていることからグラム陽性菌、グラム陰性菌、嫌気性菌のすべてに有効で、複数菌による混合感染症、あるいは原因菌の薬剤感受性試験の結果がでるまでの、病初期あるいは急性期の感染症にはしばしば使われる薬剤です。わが国では使用量が多いことからメタロβ-ラクタマーゼ産生菌が多いといわれます。今後もカルバペネム系抗生物質を安易に使用し続けるといずれ病原菌の耐性菌を生み出す危険性があります。
薬剤を服用する一般的な注意としては、もらった抗生物質を途中でやめたり、飲んだり飲まなかったりというようなことをすると、体内における薬剤濃度が低下し、耐性度が上昇したり、その薬剤に耐性の細菌を選択的に増殖させることになります。さらに畜産や養殖漁業にはヒトでの使用量を上回る量の抗生物質が使われていますが、現在,ヒトの治療に大切なバンコマイシンやニューキノロン系、カルバペネム系薬剤など(化学構造が類似の薬剤も含む)の使用制限をする事も大切と思われます。すでにこれらの抗菌薬を服用したことがない健康人がβ-ラクタマーゼ産生細菌を保菌していることが確認されていることは、その環境汚染菌が飲食物を介して侵入していることを示唆しています。現在のところNDM-1は外国由来菌でありますが、容易に他の細菌に伝達可能な耐性遺伝子であることを考えると、常に出現の有無を監視することが必要と思われます。
獣医師、医学博士 小林 一寛


